Kein einheitliches Bild zum möglichen Biologika-Austausch
Bereits seit 5 Jahren finden Ärztinnen und Ärzte Hinweise für eine wirtschaftliche Verordnungsweise von Biologika und Biosimilars in der Arzneimittel-Richtlinie (AM-RL § 40a). 2023 folgten dann die ersten Regelungen für die Austauschbarkeit von Biologika in Apotheken. Diese betreffen zunächst aber ausschließlich Zubereitungen aus Fertigarzneimitteln, also zumeist patientenindividuell von Apotheken hergestellte Infusions- oder Injektionslösungen, die die Patientin oder der Patient unmittelbar in der Arztpraxis verabreicht bekommt (§ 40b AM-RL). Nun hat der G-BA ein Stellungnahmeverfahren zur Einführung eines weiteren Paragrafen in der AM-RL eröffnet. Dieser beschäftigt sich mit dem Austausch der restlichen Biologika, die als Fertigarzneimittel an Patientinnen und Patienten abgegeben werden (geplanter § 40c AM-RL). Demnach könnte in Zukunft auch bei Biologika-Fertigarzneimitteln ein Austausch in der Apotheke stattfinden, ähnlich, wie es bereits bei Generika der Fall ist.1
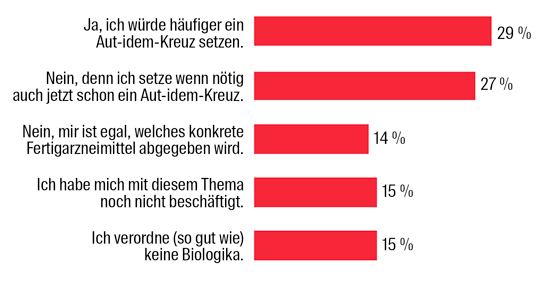
Eine Umfrage des DeutschenArztPortals2 (n = 137) zeigt kein einheitliches Bild zur Frage, ob ein Austausch in der Apotheke Auswirkungen auf das Verordnungsverhalten hätte. 29 % der Befragten geben an, dass sie in diesem Fall häufiger ein Aut-idem-Kreuz setzen würden, 27 % setzen auch heute schon ein Kreuz, wenn sie es für nötig halten.
Hätte ein Austausch von Biologika-Fertigarzneimitteln in der Apotheke ähnlich wie bei Generika Auswirkungen auf Ihr Verordnungsverhalten?
1 G-BA-Beschluss vom 11.06.2025 zur Einleitung eines Stellungnahmeverfahrens (https://www.g-ba.de/beschluesse/7255/)
2 Arztumfrage im Rp. Praxis-Newsletter des DeutschenArztPortals vom 08.07.2025 bis 20.07.2025
